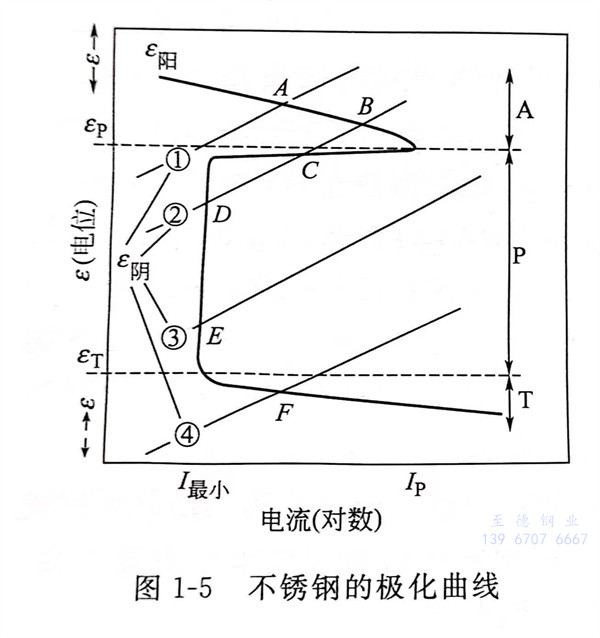
不銹鋼的極化曲線,見圖1-5。圖1-5描述了不銹鋼以及有活化、鈍化轉變的合金電極動力學過程,并按電位分為活化區(A)、鈍化區(P)和過鈍化區(T)。應用陽極極化曲線((E陽))及相關的陰極極化曲線(圖1-5中的①、②、③、④)可以求得腐蝕電位和腐蝕電流密度(圖1-5中的陽極極化曲線和陰極極化曲線的交點A、B、C、D、E、F)。
金(jin)(jin)屬或合金(jin)(jin)在不(bu)同條(tiao)件下,其電(dian)(dian)(dian)化(hua)(hua)學腐(fu)(fu)蝕有(you)四種(zhong)狀(zhuang)態(tai)(tai):一(yi)是(shi)(shi)活化(hua)(hua)狀(zhuang)態(tai)(tai),腐(fu)(fu)蝕電(dian)(dian)(dian)流(liu)強度(du)較(jiao)大,因而腐(fu)(fu)蝕速度(du)較(jiao)快(kuai);二是(shi)(shi)相對穩(wen)(wen)定狀(zhuang)態(tai)(tai),即(ji)金(jin)(jin)屬處于(yu)可以鈍(dun)化(hua)(hua)也(ye)(ye)可以活化(hua)(hua)狀(zhuang)態(tai)(tai);三是(shi)(shi)鈍(dun)化(hua)(hua)穩(wen)(wen)定狀(zhuang)態(tai)(tai),金(jin)(jin)屬只處于(yu)鈍(dun)化(hua)(hua)狀(zhuang)態(tai)(tai),而且是(shi)(shi)穩(wen)(wen)定的(de),能夠自動鈍(dun)化(hua)(hua),只有(you)很小(xiao)的(de)腐(fu)(fu)蝕電(dian)(dian)(dian)流(liu),腐(fu)(fu)蝕速度(du)很小(xiao);四是(shi)(shi)過(guo)鈍(dun)化(hua)(hua)狀(zhuang)態(tai)(tai),當金(jin)(jin)屬處于(yu)過(guo)鈍(dun)化(hua)(hua)狀(zhuang)態(tai)(tai)時有(you)較(jiao)高(gao)的(de)腐(fu)(fu)蝕電(dian)(dian)(dian)流(liu),不(bu)銹(xiu)鋼(gang)也(ye)(ye)是(shi)(shi)如此。
為了提(ti)高不(bu)(bu)銹鋼(gang)的(de)耐腐(fu)蝕(shi)性能,一般(ban)希望:不(bu)(bu)銹鋼(gang)易處于鈍(dun)(dun)化狀(zhuang)態(tai)(tai),也就(jiu)是可以(yi)自動鈍(dun)(dun)化;不(bu)(bu)銹鋼(gang)鈍(dun)(dun)化后腐(fu)蝕(shi)電(dian)流密度要很低;不(bu)(bu)銹鋼(gang)鈍(dun)(dun)化狀(zhuang)態(tai)(tai)的(de)(腐(fu)蝕(shi))電(dian)位(wei)范圍要寬。
上(shang)述三(san)點(dian)分別(bie)指出(chu)了不銹鋼獲(huo)得(de)鈍化的必要條(tiao)件、鈍化狀(zhuang)態(tai)的腐(fu)蝕速度和鈍化狀(zhuang)態(tai)的相對穩定(ding)性。
不(bu)(bu)銹(xiu)鋼只有處在鈍(dun)化狀(zhuang)態(tai)方(fang)能耐腐蝕(shi),這時鈍(dun)化狀(zhuang)態(tai)腐蝕(shi)電流最小,腐蝕(shi)速(su)(su)度最慢,其他(ta)三種狀(zhuang)態(tai)下(xia)(xia)不(bu)(bu)銹(xiu)鋼都是(shi)(shi)不(bu)(bu)耐腐蝕(shi)的。由此可(ke)見(jian),不(bu)(bu)銹(xiu)鋼的“不(bu)(bu)銹(xiu)”是(shi)(shi)相對的,只是(shi)(shi)在鈍(dun)化狀(zhuang)態(tai)下(xia)(xia),腐蝕(shi)速(su)(su)度比(bi)較慢。
保持不銹鋼耐腐蝕性的重要物質是鈍化薄膜。不銹鋼的表面本來就會形成這種毫微級的鈍化薄膜。現已明確,這種毫微級的鈍化薄膜是以在鉻的氧化物(Cr2O3)和氫氧根離子(OH-)結合后,進而加入水(H2O)的水合氫氧化鉻化合物為主體的物質。
在中性的(de)水溶(rong)液或硝酸(suan)中,不(bu)銹鋼(gang)的(de)鈍(dun)化(hua)薄(bo)膜(mo)(mo)非常穩定(ding)。即(ji)使(shi)是由于劃(hua)傷或破損(sun)等原(yuan)因(yin),使(shi)一部分薄(bo)膜(mo)(mo)被(bei)破壞了(le),它還(huan)具有立即(ji)再(zai)生和(he)恢(hui)復的(de)功能(neng)。前面談到的(de)環(huan)(huan)境氧化(hua)作用是指從(cong)金屬(shu)原(yuan)子中釋(shi)放電子的(de)反應,如果人為(wei)地借助于外部電源,將(jiang)“試驗(yan)(yan)金屬(shu)”置于“試驗(yan)(yan)溶(rong)液”中作為(wei)電解陽極并(bing)通電流(liu),此時就能(neng)求出電位(wei)(氧化(hua)力)與電流(liu)(腐蝕速度)的(de)相(xiang)關曲(qu)線和(he)環(huan)(huan)境的(de)氧化(hua)力強度。這個曲(qu)線稱為(wei)陽極分極曲(qu)線,如圖(tu)1-5所(suo)示。
由圖1-5可(ke)以看出,隨著電(dian)(dian)(dian)位的升高,先是(shi)(shi)陽極(ji)氧化(hua)(hua)(hua)反應(ying)(ying)(溶解反應(ying)(ying))呈(cheng)增強趨勢(shi);接下(xia)來是(shi)(shi)“活(huo)化(hua)(hua)(hua)狀態(tai)”電(dian)(dian)(dian)位區的電(dian)(dian)(dian)流(liu)(liu)增加(jia);然后(hou)是(shi)(shi)不(bu)依賴(lai)于電(dian)(dian)(dian)位增加(jia)顯示小電(dian)(dian)(dian)流(liu)(liu)的“鈍化(hua)(hua)(hua)狀態(tai)”電(dian)(dian)(dian)位區;最后(hou)再次出現隨著電(dian)(dian)(dian)位的增加(jia)的“過鈍化(hua)(hua)(hua)狀態(tai)”電(dian)(dian)(dian)位區。這里(li)的腐蝕電(dian)(dian)(dian)位Ecorr是(shi)(shi)成為(wei)陽極(ji)電(dian)(dian)(dian)流(liu)(liu)和陰極(ji)電(dian)(dian)(dian)流(liu)(liu)相(xiang)等條件的電(dian)(dian)(dian)位。
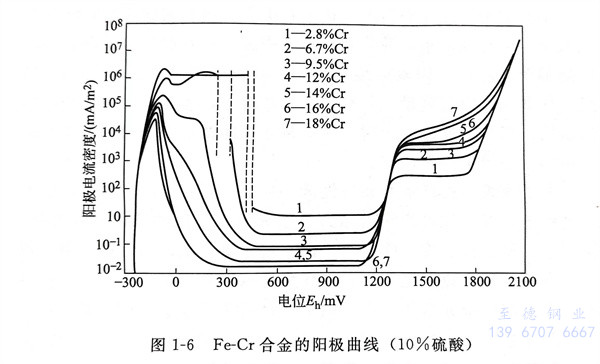
增(zeng)加鋼(gang)的(de)(de)鉻(ge)含量(liang),則陽極(ji)分極(ji)曲(qu)線的(de)(de)變化(hua)如圖1-6所示。因鉻(ge)的(de)(de)含量(liang)增(zeng)加,最大(da)陽極(ji)溶解電(dian)(dian)流及(ji)靜態(tai)(tai)區(qu)的(de)(de)陽極(ji)電(dian)(dian)流趨向于減少。不銹鋼(gang)的(de)(de)鉻(ge)(Cr)含量(liang)在12%以(yi)上時,不銹鋼(gang)易(yi)于從(cong)活性狀態(tai)(tai)向鈍化(hua)狀態(tai)(tai)轉移而(er)呈(cheng)現穩定(ding)的(de)(de)鈍化(hua)狀態(tai)(tai)。