根據電化學腐蝕原理,腐蝕過程中產生的電流大小可以代表腐蝕速率。由于陽極極化和陰極極化使腐蝕電池電位減小,從而降低腐蝕速率。產生陽極極化的主要原因是在腐蝕過程中,當溶液中有氧化劑時,在陽極表面產生了保護性的氧化膜,使金屬鈍化。其電位正移可達0.2~2V,可使腐蝕速率降低幾個數量級。
工業上廣泛應用(yong)的鐵、鉻、鎳、鈦及其(qi)合金的活化(hua)(hua)(hua)(hua)-鈍(dun)化(hua)(hua)(hua)(hua)曲(qu)線(xian)具有特殊的形式,它們的活化(hua)(hua)(hua)(hua)-鈍(dun)化(hua)(hua)(hua)(hua)轉(zhuan)變的陽(yang)極(ji)(ji)(ji)極(ji)(ji)(ji)化(hua)(hua)(hua)(hua)曲(qu)線(xian)如圖9.1所示。圖中(zhong)有三個不(bu)同(tong)電(dian)(dian)(dian)(dian)化(hua)(hua)(hua)(hua)學(xue)行為(wei)區(qu)(qu)(qu)域(yu):活化(hua)(hua)(hua)(hua)區(qu)(qu)(qu)A、鈍(dun)化(hua)(hua)(hua)(hua)區(qu)(qu)(qu)P和過鈍(dun)化(hua)(hua)(hua)(hua)區(qu)(qu)(qu)T。由于極(ji)(ji)(ji)化(hua)(hua)(hua)(hua)的作用(yong),隨著腐(fu)蝕(shi)電(dian)(dian)(dian)(dian)流(liu)強(qiang)(qiang)度(du)(du)的增加,陽(yang)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位E。升高(gao),當陽(yang)極(ji)(ji)(ji)極(ji)(ji)(ji)化(hua)(hua)(hua)(hua)曲(qu)線(xian)達(da)到最大(da)值(zhi),相應電(dian)(dian)(dian)(dian)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位為(wei)Ep,電(dian)(dian)(dian)(dian)流(liu)強(qiang)(qiang)度(du)(du)為(wei)Ip時,產生了陽(yang)極(ji)(ji)(ji)鈍(dun)化(hua)(hua)(hua)(hua),陽(yang)極(ji)(ji)(ji)過程受到極(ji)(ji)(ji)大(da)障礙,此時電(dian)(dian)(dian)(dian)流(liu)強(qiang)(qiang)度(du)(du)突然下降(jiang)到最小(xiao)值(zhi)I最小(xiao),Ep稱為(wei)初始鈍(dun)化(hua)(hua)(hua)(hua)電(dian)(dian)(dian)(dian)位,Ip稱為(wei)臨(lin)界電(dian)(dian)(dian)(dian)流(liu)強(qiang)(qiang)度(du)(du)。在很寬的陽(yang)極(ji)(ji)(ji)電(dian)(dian)(dian)(dian)位范圍內極(ji)(ji)(ji)化(hua)(hua)(hua)(hua)時,一(yi)直保持I最小(xiao)的腐(fu)蝕(shi)電(dian)(dian)(dian)(dian)流(liu)強(qiang)(qiang)度(du)(du),此時腐(fu)蝕(shi)速率大(da)大(da)降(jiang)低,陽(yang)極(ji)(ji)(ji)處于鈍(dun)化(hua)(hua)(hua)(hua)區(qu)(qu)(qu)P。
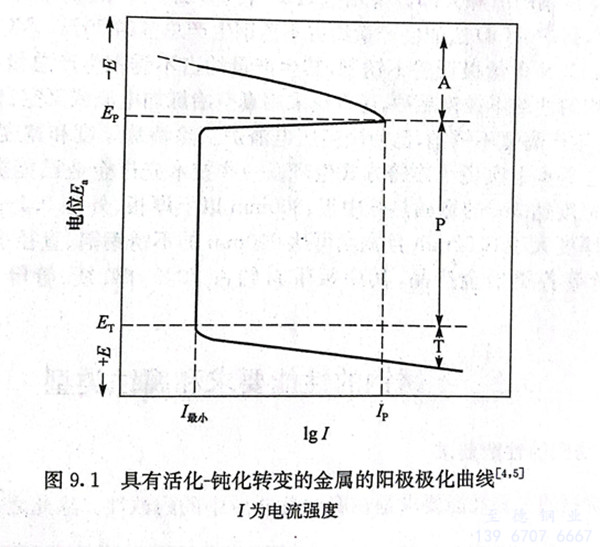
陽極電位(wei)超過(guo)Er后,腐(fu)(fu)蝕電流又(you)增加,這種現象稱為過(guo)鈍(dun)(dun)化。ET稱為過(guo)鈍(dun)(dun)化電位(wei),陽極處于過(guo)鈍(dun)(dun)化區(qu)T,此時金(jin)屬的腐(fu)(fu)蝕速(su)率(lv)又(you)增加。
根據具有活(huo)化(hua)-鈍(dun)化(hua)轉變的金(jin)(jin)屬或合金(jin)(jin)的陽極極化(hua)曲線(xian)和陰極極化(hua)曲線(xian)的相對位(wei)置(zhi),可以(yi)分析該金(jin)(jin)屬和合金(jin)(jin)鈍(dun)化(hua)狀態的穩定性。



