1973年,伊文斯等人提出不銹鋼著(zhu)色(se)膜生成原理,當不銹鋼浸入鉻酸和硫酸組成的著色液,在不銹鋼表面上發生電化學反應,見圖8-3,不銹鋼金屬(M)鉻、鎳、鐵等在陽極區放出電子變成金屬離子(M2+)。
陽極區: M→M2++2e (8-1) (M代表Cr、Ni、Fe)
在陰極區含六價鉻的鉻酸接收電子變成三價鉻(Cr3+),反應式如下:
陰極區: HCrO-4+7H++3e → Cr3++4H2O (8-2)
當不銹鋼在溶液中浸漬一段時間后,在金屬/溶液界面上金屬離子(M2+)和Cr3+的濃度達到臨界值,并超過了富鉻的尖晶石氧化物的溶解度,由于水解反應而形成氧化膜,反應式如下:
pM2++qCr3++rH2O → MpCrgOq+2rH+(8-3)
其(qi)中(zhong) 2p+3q=2r (8-4)
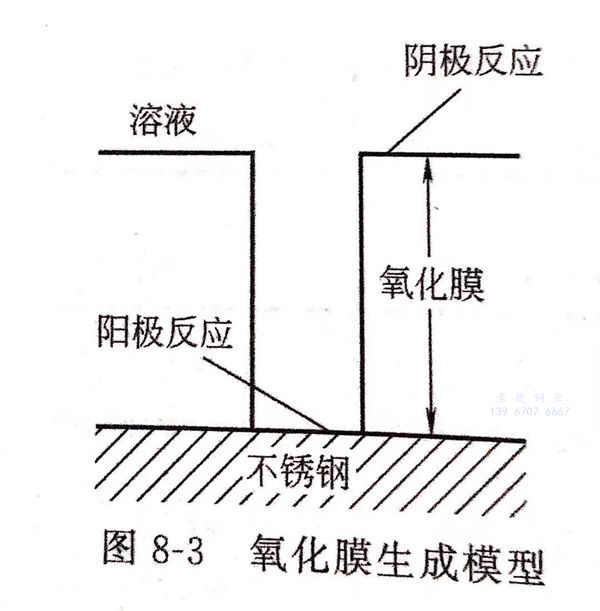
當(dang)氧(yang)化膜(mo)一旦生(sheng)成,陽極(ji)反(fan)應(ying)(ying)(ying)和陰(yin)極(ji)反(fan)應(ying)(ying)(ying)立即(ji)分離,如圖8-3所示,此時,陽極(ji)反(fan)應(ying)(ying)(ying)仍(reng)在氧(yang)化膜(mo)的孔(kong)(kong)底部(bu)即(ji)不銹鋼表面進(jin)行(xing),陰(yin)極(ji)反(fan)應(ying)(ying)(ying)在膜(mo)的表面進(jin)行(xing)。陽極(ji)反(fan)應(ying)(ying)(ying)產物(wu)M2+通(tong)過微孔(kong)(kong)向外擴(kuo)散,在孔(kong)(kong)口和孔(kong)(kong)底之間存在擴(kuo)散電位(wei)差(cha)Δφ,隨著(zhu)膜(mo)的加厚,Δφ增大。膜(mo)厚不同(tong)就產生(sheng)不同(tong)的干涉(she)色,這(zhe)就是控制(zhi)電位(wei)差(cha)可著(zhu)彩(cai)色的基本原理(li)。



